 Actualmente existen muchas técnicas para controlar la infección causada por el virus del Síndrome Reproductivo y Respiratorio del Cerdo (PRRSV). Entre ellas se encuentran la aclimatación de primerizas, la vacunación masiva de los reproductores y el cierre de granja entre otras. Pero ¿cómo podemos saber si la(s) estrategias que hemos implementado en nuestra piara han sido efectivas para controlar la infección del PRRSV?, en otras palabras, ¿cómo hemos logrado la estabilización del hato reproductor?
Actualmente existen muchas técnicas para controlar la infección causada por el virus del Síndrome Reproductivo y Respiratorio del Cerdo (PRRSV). Entre ellas se encuentran la aclimatación de primerizas, la vacunación masiva de los reproductores y el cierre de granja entre otras. Pero ¿cómo podemos saber si la(s) estrategias que hemos implementado en nuestra piara han sido efectivas para controlar la infección del PRRSV?, en otras palabras, ¿cómo hemos logrado la estabilización del hato reproductor?
Empecemos por definir que es un hato estable. Un hato estable es aquel que no presenta signos clínicos (abortos, aumento en la mortalidad de reproductoras y lechones en maternidad, aumento en el porcentaje de momias y nacidos muertos, etc.), con una producción estable y que produzca animales negativos en el momento del destete.
Estrategias diagnósticas para comprobar la estabilidad del hato reproductor
Actualmente se recomiendan tres estrategias diagnósticas para comprobar la estabilidad del hato reproductor. Recordemos que dependiendo de la técnica(s) utilizadas, la estabilidad del hato puede tardar entre 4 meses a un año después de un brote o de la implementación de la(s) técnicas recomendadas. También es importante recordar que si hemos logrado la estabilidad del hato reproductor, estamos destetando lechones negativos al PRRSV, por lo que es necesario implementar medidas de control en el cebo o de lo contrario estos animales libres del PRRSV serán nuevamente expuestos al virus y presentarán problemas clínicos severos.
1. Asegurar que se están destetando animales libres del PRRSV
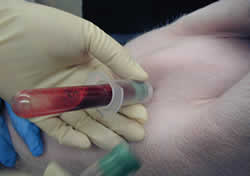 Para esto debemos sangrar durante 4 a 6 semanas por lo menos 30 lechones semanales (con un nivel de confianza del 95%, con una prevalencia >10%). Los animales ideales a muestrear son aquellos que serán destetados la semana del muestreo, ya que estos son los animales que han tenido mayor contacto con la hembra en la maternidad y tienen la mayor posibilidad de haberse contagiado con el PRRSV. Esto nos asegurará la detección de alguna hembra virémica o persistentemente infectada y que aún esta eliminando el virus. Otra población importante que debemos considerar en este muestreo son los animales que nacen débiles, los retrasados o que presentan clínica que no responde a tratamientos antibióticos. Para asegurar que la muestra sea adecuada, estos animales deben provenir de diferentes camadas. El suero de estos lechones puede mezclarse en grupos de 5 lechones por pool y deberá ser enviado para diagnóstico de PRRSV para la prueba de PCR anidada o PCR a tiempo real, ya que por ser hijos de hembras positivas, en su mayoría, estos lechones serán serológicamente positivos. Una vez que el muestreo de estas 4 a 6 semanas es negativo podemos proseguir a la segunda prueba diagnóstica.
Para esto debemos sangrar durante 4 a 6 semanas por lo menos 30 lechones semanales (con un nivel de confianza del 95%, con una prevalencia >10%). Los animales ideales a muestrear son aquellos que serán destetados la semana del muestreo, ya que estos son los animales que han tenido mayor contacto con la hembra en la maternidad y tienen la mayor posibilidad de haberse contagiado con el PRRSV. Esto nos asegurará la detección de alguna hembra virémica o persistentemente infectada y que aún esta eliminando el virus. Otra población importante que debemos considerar en este muestreo son los animales que nacen débiles, los retrasados o que presentan clínica que no responde a tratamientos antibióticos. Para asegurar que la muestra sea adecuada, estos animales deben provenir de diferentes camadas. El suero de estos lechones puede mezclarse en grupos de 5 lechones por pool y deberá ser enviado para diagnóstico de PRRSV para la prueba de PCR anidada o PCR a tiempo real, ya que por ser hijos de hembras positivas, en su mayoría, estos lechones serán serológicamente positivos. Una vez que el muestreo de estas 4 a 6 semanas es negativo podemos proseguir a la segunda prueba diagnóstica.
2. Introducción de centinelas negativos al PRRSV
Se recomienda introducir 1 centinela por cada 100 hembras en el hato reproductor. Estos animales deben provenir de un hato certificado de ser libre, no negativo al PRRSV. Generalmente, estos centinelas son machos castrados o hembras rechazadas en el proceso de selección genética. Los centinelas deben tener contacto directo (nariz con nariz) con todos los animales del hato reproductor. Normalmente se les permite caminar por los pasillos durante el día y se confinan durante la noche para evitar pleitos o destrucción de las instalaciones. Estos animales deben ser sangrados cada 15 días durante 2 meses y el suero deben ser enviado a diagnóstico para serología. Si los animales resultan positivos en cualquiera de los muestreos deben ser retirados inmediatamente. Si todos los muestreos son negativos, el último muestreo debe ser enviado a diagnóstico tanto para serología, como por PCR anidada o a tiempo real. Esto para cubrir el lapso de 10 a 14 días que existe entre el primer contacto del virus con un centinela y la producción de anticuerpos detectables mediante la prueba de ELISA. Finalmente debemos implementar la tercera prueba diagnóstica.
3. Muestreo de por lo menos 10 a 15 animales de desecho del hato reproductor
 En este caso se recomienda que se tomen animales que hayan presentado signos clínicos de PRRS. Estos animales deberán ser sacrificados y se deben tomar muestras de tonsilas y de la mayoría de los ganglios posibles (entre los más recomendables están los retrofaríngeos, los bronquiales y los inguinales). En el laboratorio de diagnóstico deben hacer un homogeneizado de la muestra y este debe ser probado contra el PRRSV por PCR anidada o a tiempo real.
En este caso se recomienda que se tomen animales que hayan presentado signos clínicos de PRRS. Estos animales deberán ser sacrificados y se deben tomar muestras de tonsilas y de la mayoría de los ganglios posibles (entre los más recomendables están los retrofaríngeos, los bronquiales y los inguinales). En el laboratorio de diagnóstico deben hacer un homogeneizado de la muestra y este debe ser probado contra el PRRSV por PCR anidada o a tiempo real.
Si estos tres muestreos son negativos, tenemos una alta probabilidad de haber logrado la estabilidad de la reproductoras. Es entonces el momento de decidir si queremos continuar con el programa de control establecido o si queremos proceder a la erradicación del PRRSV en la piara. Es importante recordar que esta decisión dependerá de la posibilidad de contar con una fuente libre de PRRSV, tanto de semen como de reposición, de la ubicación geográfica de la granja y de las medidas efectivas de bioseguridad que se puedan implementar en la granja y en el transporte para evitar la reintroducción lateral del PRRSV.




